¿Cuál es la diferencia entre calibración y validación en el laboratorio?
Si trabaja en un laboratorio, ya sea biotecnológico, farmacéutico, de I+D o clínico, es probable que conozca la necesidad de calibrar y validar sus equipos y procesos. También es probable que oiga a algunos de sus colegas utilizar las palabras indistintamente.
Aunque suenen parecidos y los procesos estén relacionados, no deben confundirse.
La calibración de equipos de laboratorio y sensores es un proceso mediante el cual se compara un valor medido con un patrón calibrado para determinar la precisión del valor medido. Algunos fabricantes prueban y calibran los equipos en la cadena de montaje y proporcionan un certificado de calibración. Este certificado sólo tiene valor si los sensores utilizados pueden ser trazables a, por ejemplo, Raad voor Accreditatie (RvA), UKAS o NIST. Sin trazabilidad, es difícil declarar un dispositivo apto para su uso, porque no se puede confiar plenamente en un valor indicado.
Aunque un dispositivo o sensor esté calibrado, esto no significa automáticamente que un equipo o una sala sean adecuados para su finalidad. El valor medido por un sensor puede ser absolutamente exacto, pero no dice nada sobre el comportamiento de una sala o un equipo en caso de diferentes cargas, cortes de electricidad o apertura de puertas. Antes de que un equipo pueda declararse apto para su finalidad, el proceso de validación tiene por objeto garantizar que una sala o dispositivo es capaz de funcionar de acuerdo con las especificaciones de las muestras que deben almacenarse en él.
Profundicemos un poco más en cada uno de ellos.
Calibración de equipos: Precisión para su laboratorio
Es probable que la báscula del cuarto de baño de su casa esté desajustada en uno o dos kilos y necesite una calibración, pero probablemente esto no le quite el sueño.
En el laboratorio, un equipo mal calibrado es directamente peligroso. Si las muestras se almacenan en una sala o un dispositivo con un sensor sin calibrar, es probable que los usuarios tomen decisiones basadas en información incorrecta. Si, por ejemplo, la sangre se guarda en un frigorífico que muestra una temperatura incorrecta, los usuarios pueden pensar que lo están haciendo todo correctamente, mientras que la sangre se almacena de forma incorrecta. Administrar esta sangre al paciente más tarde puede poner en peligro su vida. Lo mismo ocurre con los medicamentos o los alimentos.
La calibración también es necesaria para todos los sistemas de gestión de la calidad, como ISO, FDA, CAP, CLIA y GMP. Demostrar que su equipo estaba y está correctamente calibrado para cumplir las normas y reglamentos aplicables es fundamental para que un laboratorio siga avanzando.
Aunque muchos laboratorios optan por enviar sus equipos o sensores a calibrar, esto plantea muchos problemas en cuanto a su trazabilidad. ¿Cómo puede estar seguro de que un certificado de calibración de fábrica tiene algún valor? La regla general es que, sin trazabilidad NIST, un certificado de calibración de fábrica no tiene ningún valor oficial.
Dependiendo del nivel de acreditación, existen dos opciones. Si la acreditación lo permite, los usuarios pueden calibrar sus propios dispositivos con un sensor calibrado (RvA). Esto permite un buen nivel de control y una trazabilidad básica de los valores. Hay que tener en cuenta que un proceso de calibración correcto no es fácil, y no hay supervisión sobre los procesos utilizados. Esto significa que la incertidumbre de este proceso es desconocida. En otras palabras, si un usuario calibra incorrectamente los sensores, puede empeorar las cosas.
La segunda opción es contratar a una empresa profesional de calibración trazable RvA. Su personal está formado para utilizar el procedimiento correcto y no debería cometer ningún error durante el proceso. Los informes de calibración tendrán incertidumbre, lo que hace que este tipo de servicio de calibración sea muy valioso para laboratorios con altos estándares de acreditación. El inconveniente es el coste añadido de contratar a una empresa de calibración.
Independientemente de quién realice la calibración, los pasos son siempre los mismos. En primer lugar, hay que crear un entorno estable en el que se puedan comparar el sensor y el patrón. Si uno se desvía del otro, puede ser necesario compensar el sensor. Después de compensar el valor del sensor, es imprescindible repetir el proceso de calibración para comprobar que la compensación ha ajustado correctamente la lectura de la pantalla del sensor.

La colocación de sensores en un horno de bloques es un buen ejemplo de creación de un entorno estable para calibrar sensores en

Si los sensores no pueden retirarse fácilmente, la colocación de un bloque de aluminio en el interior del dispositivo mejorará considerablemente la estabilidad de las mediciones, lo que reducirá la incertidumbre.
Por último, la calibración debe notificarse correctamente. Sin una prueba escrita, cualquier calibración carecerá de valor. Un usuario tendrá que escribir correctamente qué pasos se siguieron y qué estándares se utilizaron para realizar una calibración. También tendrá que mostrar qué valores se registraron durante el proceso de calibración para informar correctamente de las compensaciones realizadas.
Validación: Cómo demostrar que algo es adecuado
En casi todos los casos, demostrar que los equipos están correctamente calibrados es un requisito previo para poder realizar la validación. Aun así, la validación es un tema mucho más amplio; también consiste en: flujos de trabajo, rendimiento del personal, calidad de los datos y mucho más.
A diferencia de los procesos de calibración de equipos específicos para cada pieza de equipo (independientemente de dónde se utilice), los procesos de validación suelen ser exclusivos de cada laboratorio y su modelo de negocio.
Mientras que, por ejemplo, al calibrar una simple báscula, una onza es una onza, independientemente de dónde o cómo se utilice la báscula. No existe un enfoque único para la validación global de laboratorios. Requiere un planteamiento y unos resultados específicos para cada empresa (en caso de problema o de auditoría en la que pueda exigirse un registro en papel).
Los procesos de validación de un laboratorio acreditado en relación con los sensores utilizados en XiltriX constan de dos partes principales. En primer lugar, hay que demostrar que el equipo y las salas funcionan de acuerdo con las especificaciones para las muestras que se van a almacenar o los medicamentos que se van a producir. El truco está en que, aunque el proceso de validación suele ser único, sigue habiendo algunas normas que todos los laboratorios deben cumplir. Por citar sólo un ejemplo, los protocolos IQ (Cualificación de la Instalación), OQ (Cualificación Operativa) y PQ (Cualificación del Rendimiento) suelen aplicarse a equipos y sistemas de software.
Brevemente, se definen del siguiente modo:
- IQ valida que los equipos estén correctamente instalados según las instrucciones del fabricante (que, naturalmente, suelen incluir también equipos calibrados según esas instrucciones).
- La OQ valida que los equipos funcionan según lo previsto dentro de un rango de operaciones especificado por el fabricante o dictado por una norma de conformidad.
- PQ integra el uso en los protocolos: ¿su equipo cumple las normas a medida que se utiliza?
Las partes OQ y PQ son las que más trabajo dan. En el ejemplo de un frigorífico de sangre, poder confiar en el valor de visualización del dispositivo es el primer paso del proceso de validación. Antes de colocarlo en el laboratorio, hay que saber si el aparato puede recuperarse con suficiente rapidez tras la apertura de una puerta. También es importante la distribución de la temperatura en el almacenamiento de muestras dentro del frigorífico. Esto puede ser diferente con distintas cargas de bolsas de sangre. Por último, es imperativo saber cuánto tiempo mantendrá la temperatura un aparato en caso de corte total del suministro eléctrico.
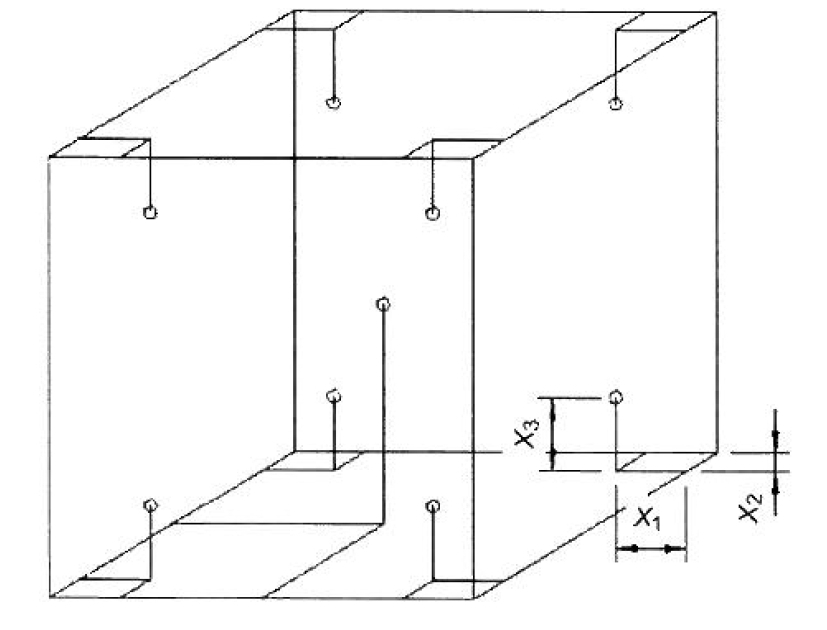
Para llevar a cabo dicha validación, se realiza un mapeo multisensor del dispositivo. El número de sensores depende de una serie de condiciones y del tamaño del dispositivo o de la sala a cartografiar. Para más detalles, véase la norma internacional NEN-EN-IEC 60068-3-5:2018. Lo más habitual son las 8 esquinas del dispositivo. El centro y la temperatura ambiente se registran durante un periodo de tiempo predeterminado (un total de 9 posiciones). A continuación, los resultados se comparan con los criterios de almacenamiento de las bolsas de sangre o las muestras que se van a almacenar. Si el dispositivo aprueba, es apto para su uso. Si falla, habrá que ajustarlo, repararlo o sustituirlo.
El mapeo de temperatura no es definitivamente la única prueba que determina si un dispositivo es adecuado para su propósito. Múltiples parámetros determinarán si las muestras pueden almacenarse adecuadamente en un dispositivo. Cosas como ser capaz de recuperarse lo suficientemente rápido después de una apertura de puerta estandarizada es uno de ellos. Otra prueba habitual consiste en comprobar el "tiempo de retención" de un dispositivo con diferentes cargas. Este tiempo determinará, si falla la alimentación, después de cuánto tiempo las muestras/sangre o los medicamentos ya no pueden utilizarse para los pacientes o suministrarse a farmacias o bancos de sangre. Disponer de un sistema de vigilancia y alarma adecuado también es un requisito previo para un sistema de gestión de la calidad.
Durante casi 40 años, XiltriX se ha centrado exclusivamente en garantizar la integridad y eficacia de los equipos, los procesos y el entorno de un laboratorio. Ayudamos a los clientes a reducir las necesidades de personal en torno a la calibración y la validación, al tiempo que aumentamos tanto la confianza como la elaboración de informes en torno a estos procesos.
HAGA CLIC EN ESTE ENLACE PARA DESCARGAR EL PDF DEL LIBRO BLANCO
Póngase en contacto con nosotros para saber cómo podemos ayudarle a acelerar y optimizar estos procesos críticos y mucho más.
Teléfono: +31-73-5212229
Correo electrónico: sales@xiltrix.com
Página web: www.xiltrix.com
Han Weerdesteyn
CCO
Enero de 2023
Si quieres saber más sobre XiltriX, házmelo saber.
Han Weerdesteyn
CCO